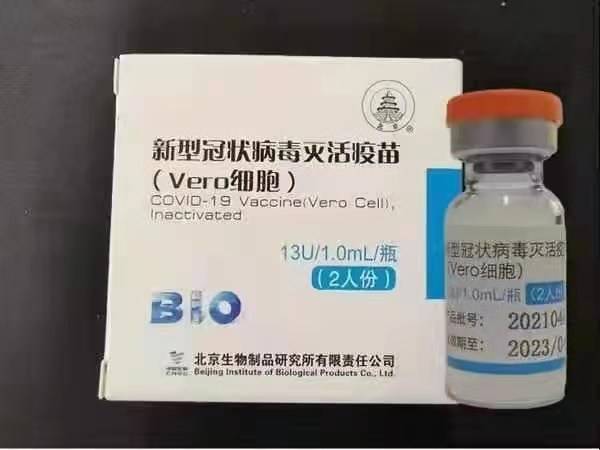
Sinopharm (Пекин): BBIBP-CorV
ЕТАП 1
1 Изпитване
ChiCTR2000032459
Китай
ЕТАП 2
2 изпитания
NCT04962906
Аржентина
ChiCTR2000032459
Китай
ЕТАП 3
6 изпитания
NCT04984408
ChiCTR2000034780
Обединени арабски емирства
NCT04612972
Перу
NCT04510207
Бахрейн, Египет, Йордания, Обединени арабски емирства
NCT04560881, BIBP2020003AR
Аржентина
NCT04917523
Обединени арабски емирства
Одобрения
Списък на СЗО за спешна употреба 59 държави
Ангола 、 Аржентина 、 Бахрейн 、 Бангладеш 、 Беларус 、 Белиз 、 Боливия (Многонационална държава) 、 Бразилия 、 Бруней Даруссалам 、 Камбоджа 、 Камерун 、 Чад 、 Китай 、 Коморски острови 、 Египет 、 Екваториална Гвинея 、 Габон 、 Гамбия 、 Грузия 、 Грузия 、 Грузия 、 Иран (Ислямска Република) 、 Ирак 、 Йордания 、 Киргизстан 、 Лаоска Народна Демократична Република
Ливан, Малайзия, Малдиви, Мавритания, Авриций, Монголия, Черна гора, Мароко, Мозамбик, Намибия, Непал, Нигер, Северна Македония, Пакистан, Парагвай, Перу, Филипини, Република Конго, Енегал, Сърбия, Сейр Острови 、 Сомалия 、 Шри Ланка 、 Тайланд 、 Тринидад и Тобаго 、 Тунис 、 Обединени арабски емирства 、 Венецуела (Боливарианска република) 、 Виетнам 、 Зимбабве
Sinopharm BBIBP-CorV COVID-19 е инактивирана ваксина, произведена от културно отглеждани вирусни частици, които нямат патогенна способност. Този кандидат за ваксина е разработен от Sinopharm Holdings и Пекинския институт по биологични продукти.
Ваксината Sinopharm BBIBP-CorV действа, като позволява на имунната система да произвежда антитела срещу SARS-CoV-2 бета коронавирус. Инактивираните вирусни ваксини се използват от десетилетия, като ваксина срещу бяс и ваксина срещу хепатит А. Тази технология за развитие е успешно приложена към много известни ваксини, като ваксината срещу бяс.
Щамът SARS-CoV-2 на Sinopharm (щам WIV04 и библиотечен номер MN996528) е изолиран от пациент в болница Jinyintan в Ухан, Китай. Вирусът се размножава в култура в компетентна клетъчна линия Vero и супернатантата на заразените клетки се инактивира с β-пропиолактон (1: 4000 об./Об., 2 до 8 ° С) за 48 часа. След изясняване на клетъчните остатъци и ултрафилтрация, беше извършено второ инактивиране на β-пропиолактон при същите условия като първото инактивиране. Според СЗО ваксината се адсорбира върху 0,5 mg стипца и се зарежда в предварително напълнени спринцовки в 0,5 ml стерилен фосфатно-буфериран физиологичен разтвор без консерванти.
На 31 декември 2020 г. Държавната администрация по лекарствата обяви одобрението на експерименталната ваксина, разработена от Sinopharm.
На 7 май 2021 г. Световната здравна организация обяви одобрението на ваксината. Списъкът на СЗО за спешна употреба даде възможност на страните да ускорят своите собствени регулаторни одобрения за внос и администриране на ваксина срещу COVID-19. Консултативната експертна група на СЗО по имунизационни стратегии също завърши своя преглед на ваксината. Въз основа на всички налични доказателства, СЗО препоръчва две дози ваксина, с интервал от три до четири седмици, за възрастни над 18 години. Ефикасността на ваксините срещу симптоматично и хоспитализирано заболяване се оценява на 79% за всички възрастови групи, взети заедно.
Американската медицинска асоциация публикува „Рандомизирано клинично изпитване: Ефект от 2 инактивирани ваксини срещу SARS-CoV-2 върху симптоматична инфекция с COVID-19 при възрастни“ на 26 май 2021 г., като заключава, че „в този предварително определен междинен анализ на рандомизирано клинично изпитване, възрастни 2-те инактивирани ваксини срещу SARS-CoV-2, приложени в този предварително определен междинен анализ на рандомизирани клинични проучвания, значително намаляват риска от симптоматичен COVID-19, а сериозните нежелани събития са редки. " В това рандомизирано проучване фаза 3 при възрастни ефикасността на 2-те инактивирани ваксини с цял вирус при симптоматични случаи на COVID-19 е съответно 72,8% и 78,1%. 2 ваксини са имали редки сериозни нежелани събития със сходна честота с контролната група само за стипца и повечето не са свързани с ваксинацията. Проучвателен анализ установи, че двете ваксини индуцират измерими неутрализиращи антитела, подобни на резултатите от изпитването фаза 1/2.
Работната група на WHO SAGE публикува преглед на ваксината Sinopharm/BBIBP COVID-19 на 10 май 2021 г. Ваксината на GAVI COVID-19 включва монитор за флакон с ваксина, който казва на здравните работници дали ваксината е била съхранявана правилно и не е била изложена на прегряване. В резултат на повреда, GAVI съобщи на 14 май 2021 г. интелигентните етикети, произведени от Zebra Technologies и направени от Temptime Corporation, се състоят от кръг с по -светъл оцветен квадрат в средата, направен от безцветен химикал, който необратимо развива цвета с течение на времето . Това става по -тъмно, за да даде визуална индикация за кумулативната топлинна експозиция. След като флаконът е бил изложен на топлина извън оптималния диапазон на съхранение, квадратът става по -тъмен от кръга, което показва, че ваксината не трябва да се използва повече.
Регистрационен номер на националната библиотека за лекарства за ваксини срещу лекарства COVID-19 BBIBP-CorV: DB15807.